隨著工業的發展,汞污染越來越嚴重。由于汞的污染特性,不易分解及轉移。造成了食品中富集了各種含汞化合物,從而導致各種慢性、急性汞中毒事件頻出。目前,食品中汞的主要存在形式可分為無機汞和有機汞兩大類,其中有機汞的毒性遠大于無機汞,無機汞主要是對腎臟有毒性作用,而有機汞主要對腦組織傷害比較大。因此對汞形態的監測顯得尤為重要。
本文參考國家衛生和計劃生育委員會發布的《GB 5009.17-2014 食品中甲基汞的測定》,通過HPLC-ICPMS聯用,采用C18柱,利用等度洗脫的方式對稀酸浸提后的大米進行了分析,同時對樣品采取了加標處理,且加標回收率良好。測試結果表明,該方法能夠快速準確地進行大米樣品中汞形態的分析。
1.儀器簡介
本方法采用Skyray Instrument LC-310E與ICP-MS 2000E聯用,采用一鍵式數據采集、精準式譜圖定位及強大的軟件譜圖處理功能,可滿足不同的形態測試需求(如圖1)。

圖1.HPLC-ICPMS聯用測汞形態的分析儀
2.測試原理
樣品溶液經過前處理,由HPLC進樣口進樣,經色譜柱分離,通過霧化器霧化后送入高溫等離子體中,干燥、原子化、電離,元素離子經接口室進入質譜儀,通過離子透鏡系統、質量分析器及檢測器,檢測器對相應元素離子做出響應(每秒離子計數cps(counts
per second),經軟件處理,響應強度和時間組成的峰面積與相應組分離子濃度成正比關系進行定性定量分析。
3.實驗部分
3.1實驗設備及試劑
液相色譜-電感耦合等離子體質譜聯用儀(江蘇天瑞儀器股份有限公司);
電子天平(BSA224S,賽多利斯);
色譜柱(Ultimate XB-C18,4.6×150mm,5μm);
超純水系統(Millipore,電阻率為18.25MΩ·cm);
鹽酸(優級純,Scharlau);
氨水(優級純,上海晶純試劑有限公司);
乙酸銨(優級純,阿拉丁化學試劑);
L-半胱氨酸(生物純,阿拉丁化學試劑);
甲醇(色譜純,Oceanpak 色譜純試劑);
汞形態標準溶液(水中汞GBW(E)083186、甲基汞GBW(E)083364、乙基汞GBW(E)081524,中國計量科學院);
超聲波(KH-500E,昆山禾創);
雙功能水浴恒溫振蕩器(SHA-B,江蘇國華);
高速離心機(TG16G,凱特)。
3.2樣品前處理
稱取大米樣品1.0g(精確至0.001g),置于15mL的離心管中,加入10mL的鹽酸溶液(5mol/L)靜置過夜。后經常溫水浴振蕩60min,于4℃下以8000r/min的轉速進行離心15min。取上層清液2mL至5mL的容量瓶中,用稀氨水調節PH到7.0,再加入0.1mL的L-半胱氨酸(10g/L),最后用超純水定容至刻度并搖勻。用0.45μm的有機系濾膜過濾后,待測。
3.3流動相及汞形態標準溶液配制
3.3.1流動相的配制
60mmol/L乙酸銨+0.1%L-半胱氨酸+5%甲醇:稱取4.627g乙酸銨,1.21gL-半胱氨酸于100mL容量瓶中,加入少量的超純水并于電熱板上加熱使其完全溶解,冷卻后定容至100mL。將定容好的溶液移入1000mL的淋洗液瓶中,同時加入50mL的甲醇,定容至1L。經0.45μm的有機系濾膜過濾后,于超聲波超聲脫氣30min,現用現配。
3.3.2汞形態標準溶液:
三種汞標準溶液采用淋洗液按照梯度濃度的方式依次被稀釋為1.0μg/L、2.0.μg/L、4.0μg/L、8.0μg/L、10.0μg/L 混合標準溶液,同時配制5μg/L三種汞形態的單標溶液,用來判別每種汞形態的出峰時間。
3.4實驗條件
3.4.1色譜條件
色譜條件詳見表1。
表1. HPLC分析條件
|
參數
|
參數設定
|
|
色譜柱
|
Ultimate XB-C18,5μm,150×4.6mm。
|
|
流動相
|
60mmol/L乙酸銨+0.1%L-半胱氨酸+5%甲醇(pH=7.0)。
|
|
流 速
|
1.0mL/min
|
|
柱 溫
|
25℃
|
|
進樣量
|
100μL
|
|
洗脫程序
|
等度洗脫
|
3.4.2質譜條件
ICP-MS分析條件見表2。
表2.ICP-MS分析條件
|
參數
|
參數設定
|
參數
|
參數設定
|
|
功 率
|
1300W
|
等離子氣
|
13L/min
|
|
輔助氣
|
1.06L/min
|
載 氣
|
1.2L/min
|
|
采樣深度
|
16
|
分析模式
|
標準模式
|
|
待測質量數
|
202
|
駐留時間
|
10ms
|
3.5實驗結果
3.5.1標準曲線
按照混合標準溶液濃度1.0μg/L、2.0.μg/L、4.0μg/L、8.0μg/L、10.0μg/L 進樣得到色譜圖,計算其峰面積,以濃度和峰面積繪制標準曲線,線性相關系數均大于0.999,結果詳見圖2-1~2-3。
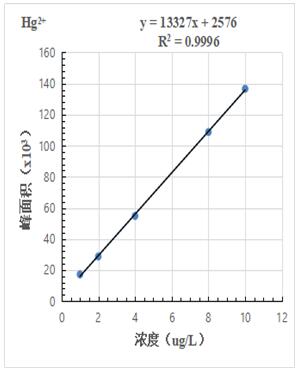
圖2-1.Hg2+標準曲線
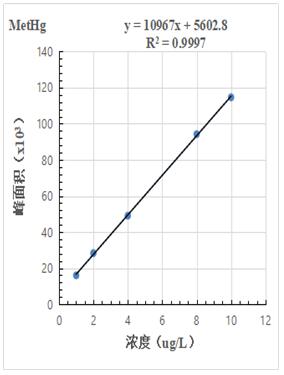
圖2-2.MetHg標準
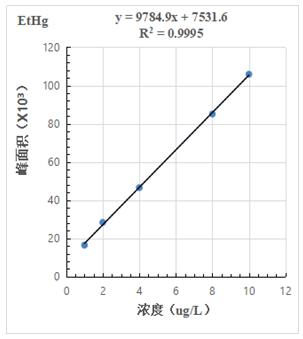
圖2-3.EtHg標準曲線
3.5.2色譜分離圖
1.0μg/L、2.0.μg/L、4.0μg/L、8.0μg/L、10.0μg/L 汞形態混合標準溶液分離色圖譜如圖3所示,其中無機汞(Hg2+)、甲基汞(MetHg)、乙基汞(EtHg)相對保留時間分別為118s、185s、379s,從譜圖疊加圖上可以看出,三種汞形態出峰時間穩定,且分離度較好。
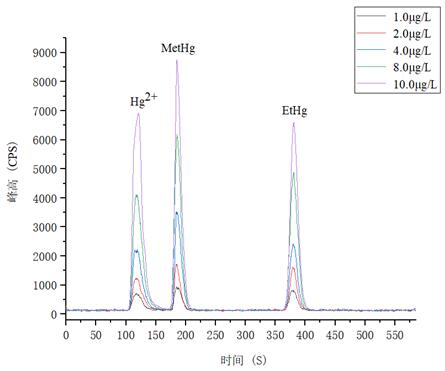
圖3. 汞形態混合標準溶液分離圖譜
3.5.3 檢出限
如圖4所示為1.0μg/L汞形態混和標準溶液分離圖譜,以各形態峰附近基線處的3倍信噪比(S/N)峰高對應的濃度作為檢出限,溶液中Hg2+、MetHg、EtHg分別為0.112μg/L、0.0718μg/L、0.0698μg/L。
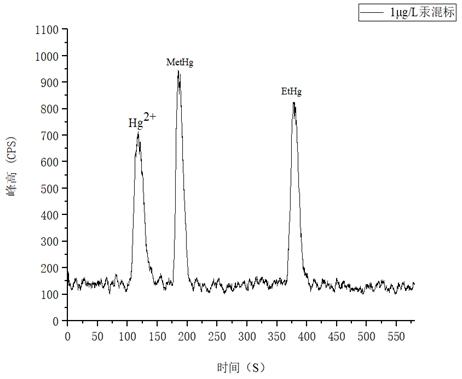
圖4. 1.0μg/L汞形態混合標準溶液圖譜
3.5.4 測試結果
以大米樣品為試樣,進行稀酸浸提,同時為了考察方法的準確性,并對大米試樣采取了加標的方式,測試結果詳見表3。
表3 大米樣品及樣品加標結果
|
組分名稱
|
稀釋后濃度
|
原液濃度
|
加標后濃度
|
加標回收率
|
|
(μg/L)
|
(μg/kg)
|
(μg/L)
|
(%)
|
|
無機汞
|
0.227
|
5.68
|
5.84
|
112
|
|
甲基汞
|
未檢出
|
ND
|
4.50
|
90
|
|
乙基汞
|
未檢出
|
ND
|
4.67
|
93
|
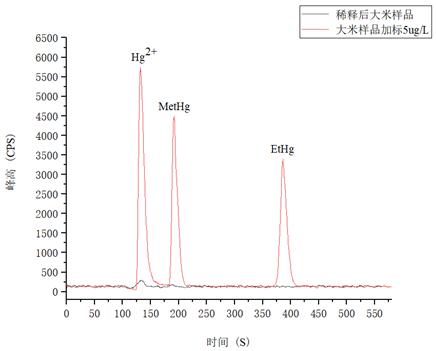
圖5. 大米樣品及樣品加標5.0μg/L圖譜
4. 結論
本文建立了LC-ICPMS測試大米中汞形態的分析方法,結果表明該方法檢出限低、測試結果準確,其加標回收率在90%~112%之間,線性相關系數均在0.999以上;同時汞的三種形態能夠在8min左右完成,且分離度較好,該方法可滿足食品中大米樣品汞形態分析的要求。
5.參考文獻
[1] 國家衛生和計劃生育委員會發布 GB 5009.17-2014食品安全國家標準 食品中甲基汞的測定 液相色譜-原子熒光光譜聯用方法,2015。